金桔
金币
威望
贡献
回帖0
精华
在线时间 小时
|
登陆有奖并可浏览互动!
您需要 登录 才可以下载或查看,没有账号?立即注册


×
心血管疾病是一组心脏和血管失调,包括冠心病、脑血管疾病、外周动脉疾病等,是全球死亡的主要原因。蛋白质组学作为一门高通量的生物分析技术,在心血管疾病领域的应用日益广泛。通过对生物样本中蛋白质的全面分析,蛋白质组学为心血管疾病的发病机制研究、生物标志物发现、风险评估与预测以及药物治疗效果评估等提供了强有力的工具。本期将基于2024年度国内外发表的重要研究成果,探讨基于SomaScan平台的蛋白质组学检测在心血管疾病领域中的应用进展。
01
在心血管疾病发病机制与信号通路中的应用
在一项多中心病例对照研究中,研究人员利用SomaScan平台对99例肥厚型心肌病(HCM)患者和15例非心脏疾病对照组的心肌样本进行了全分析,涵盖了7289种蛋白质。研究发现,HCM患者的多种信号通路存在失调,包括新发现的Ras-MAPK通路、泛素介导蛋白降解通路、血管内皮生长因子相关通路等,以及已知的代谢通路、炎症通路、纤维化通路等[1]。值得注意的是,Ras-MAPK通路在HCM的发生和发展过程中扮演着重要角色,与病情的严重程度密切相关。另有一项多中心病例对照研究对402名HCM患者进行了分析,探寻与既往心血管事件(MACE)相关的信号转导途径。研究发现,相较于无MACE历史的患者,有MACE历史的HCM患者在TGF-β、Ras-MAPK和PI3K-Akt等信号转导途径上存在显著差异[2]。这些发现有助于深入理解HCM的发病机制和疾病进展,为开发更有效的治疗策略提供了重要依据。
此外,一项前瞻性多中心队列研究采用血液中蛋白质组学分析方法,对284名HCM患者进行了新发心房颤动(AF)风险的预测。研究将患者分为训练集和测试集,并成功发现了一种基于12种蛋白质的预测模型,该模型能够有效预测HCM患者的新发AF风险。进一步的研究分析还识别出了与新发AF密切相关的信号通路,尤其是Ras-MAPK途径及其上下游通路的异常激活,这暗示了这些通路可能在HCM患者向AF进展的过程中发挥了关键作用[3]。该研究成果不仅为HCM患者提供了一种新颖的AF风险评估工具,也为深入理解HCM相关AF的发生机制提供了新的视角。
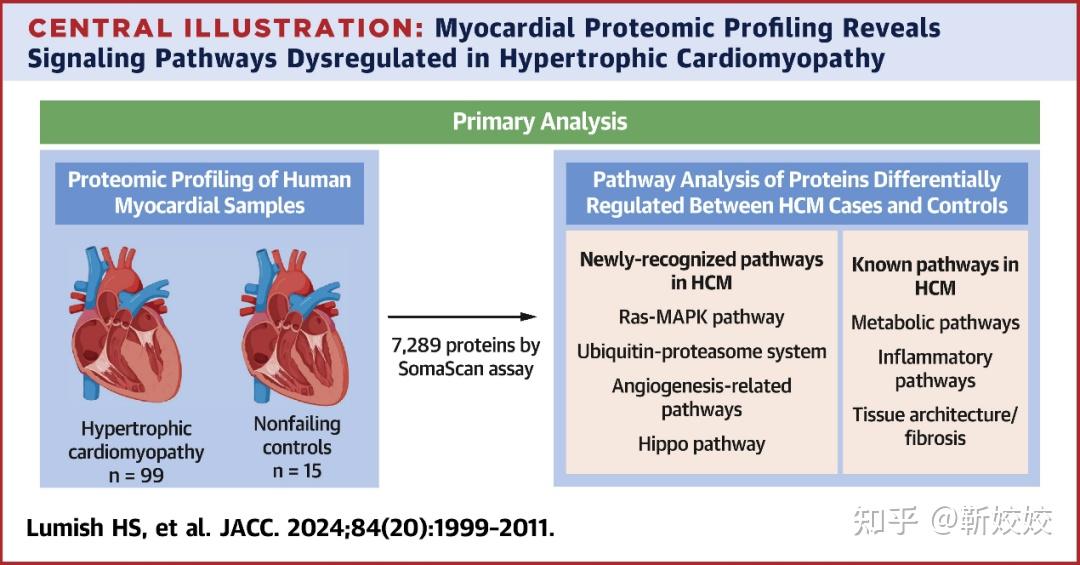
图1. 心肌蛋白质组学分析揭示肥厚性心肌病中的信号通路失调[1]
另一方面,研究人员利用大规模基因组学和蛋白质组学数据,研究人员在81190例静脉血栓栓塞(VTE)病例和1419671名对照中识别出VTE相关遗传变异。随后,在35559人的血液蛋白数据中验证了这些变异的效应,发现34种蛋白质与VTE显著关联。研究进一步探讨了这些蛋白质在可调节风险因素(如肥胖、吸烟、失眠)与VTE间的介导作用,并评估了其药物开发潜力。部分蛋白质还与心血管疾病相关,提示存在共同分子机制,这些发现对理解VTE发病机制及制定预防策略的重要性[4]。
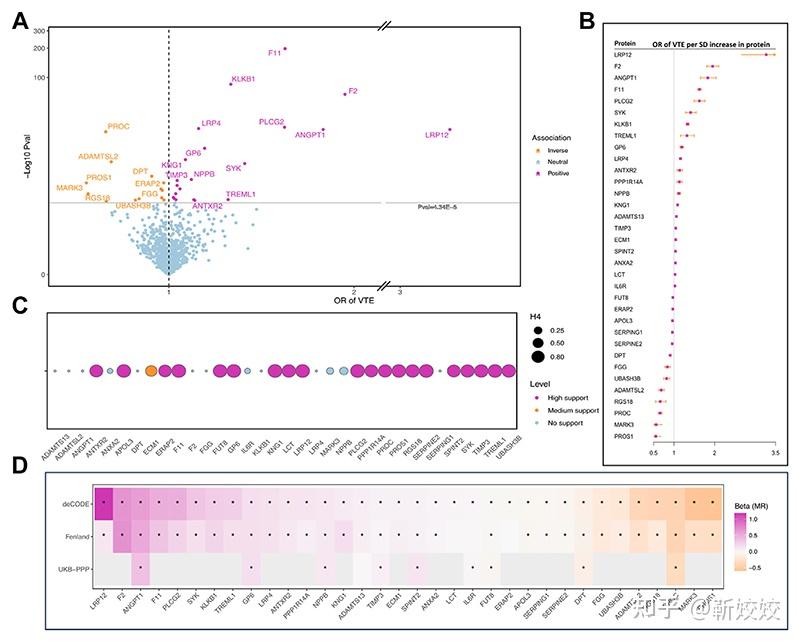
图2. 血液蛋白与VTE风险之间的关系[4]
02
在心血管疾病治疗靶点与药物研发中的应用
通过大规模蛋白质组学与遗传学的整合研究,研究人员利用孟德尔随机化(MR)方法及共定位分析,揭示了众多心血管疾病的潜在治疗靶点。Zhu等[5]在心脏疾病、中风、心力衰竭等多个领域发现了7种多效用治疗蛋白和39种特定靶标蛋白质,其中PILRA蛋白被证实与心脏病和阿尔茨海默病存在密切关联,为跨疾病治疗提供了新线索;Shi等[6]专注于非缺血性心肌病(NISCM)的研究,鉴定了LILRA5和NELL1等蛋白质与NISCM的显著相关性,为NISCM的潜在治疗提供了新靶点;Chen等[7]系统性地探讨了冠状动脉钙化(CAC)的潜在治疗靶点,最终确定IGFBP3、ABCC6、ULK3、DOT1L、KLB和AMH为值得进一步探究的潜在治疗靶点,为CAC的防治提供了新思路;Alcalde-Herraiz等[8]探讨了遗传因素预测的sclerostin水平对心血管生物标志物、风险因素及疾病结局的影响,结果显示,较低的sclerostin水平增加了冠状动脉疾病和2型糖尿病的风险,为理解sclerostin在心血管疾病中的作用提供了新证据。
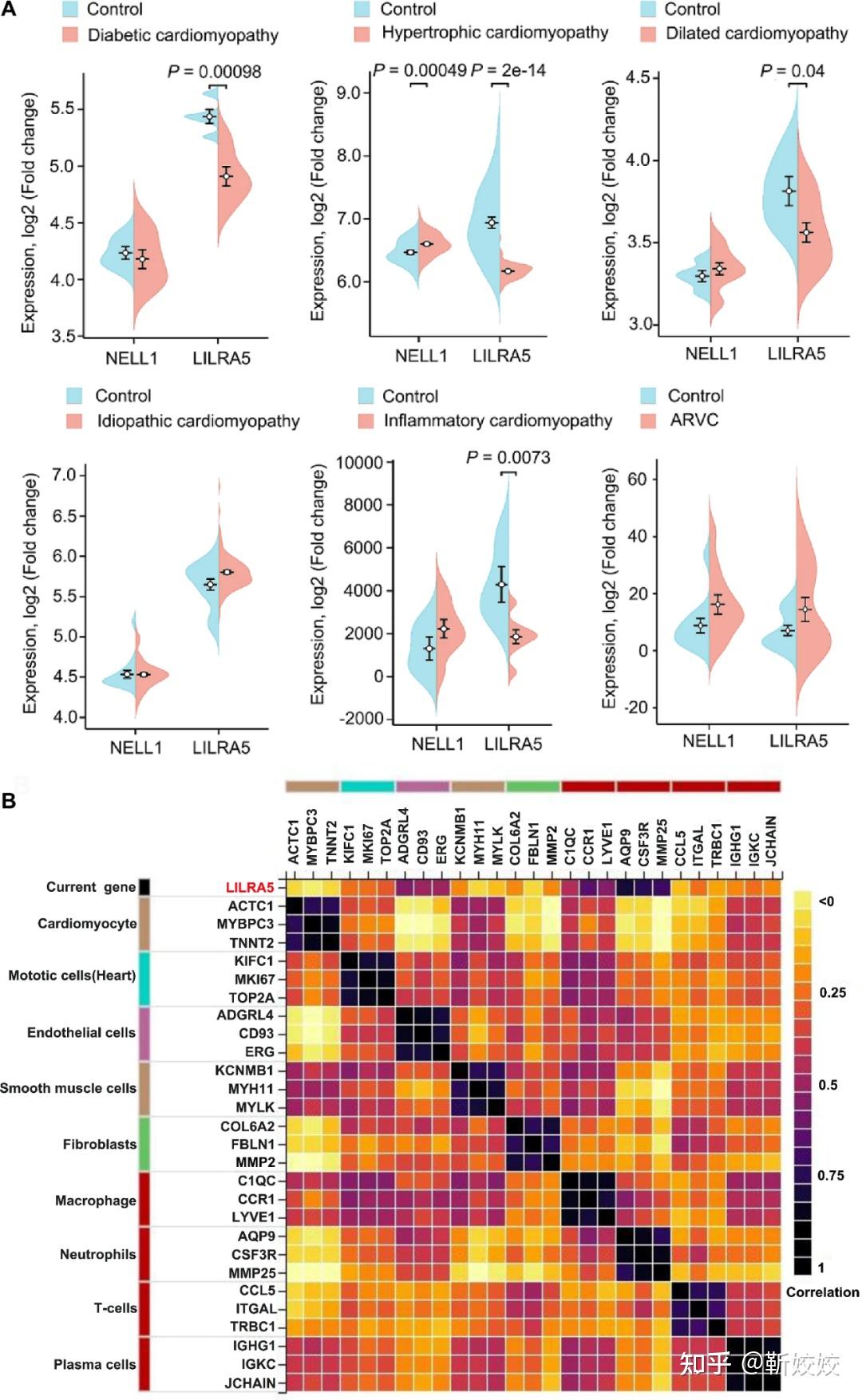
图3. LILRA5和NELL1在NISCM亚型中的表达及正常心肌中LILRA5的细胞相关性[6]
此外,Abou Kamar等[9]利用173名慢性心力衰竭(HFrEF)患者的血液样本和心脏超声检查数据,探讨了循环系统中蛋白质水平与左心室(LV)及左心房(LA)功能参数之间的关联。研究发现,与左心室功能相关的蛋白质主要反映了自主神经系统的活动状况,而与左心房功能密切相关的蛋白质则主要涉及细胞外基质的代谢过程。进一步调整左心室射血分数后,研究揭示了fibulin-5和HSP40等与左心房扩张特定相关的蛋白质,为HFrEF的精准诊断和治疗提供了潜在生物标志物。
同时,Diakos等[10]对11名接受体外膜氧合或轴流泵支持的急性心源性休克患者的血浆样本进行了蛋白组学分析,涉及1305种蛋白质。研究发现,机械辅助循环后,患者血浆中的炎症标志物和促炎细胞死亡蛋白水平明显降低。尽管两种设备生物效应相似,但在具体影响的蛋白质上存在差异,暗示治疗机制具有异质性。进一步生化网络分析显示,EGR1和IkBKB是调节炎症反应的关键上游分子,其下调可能是辅助循环改善炎症状态的机制。这些发现加深了对心源性休克的理解,并为开发针对性治疗提供了潜在靶点。
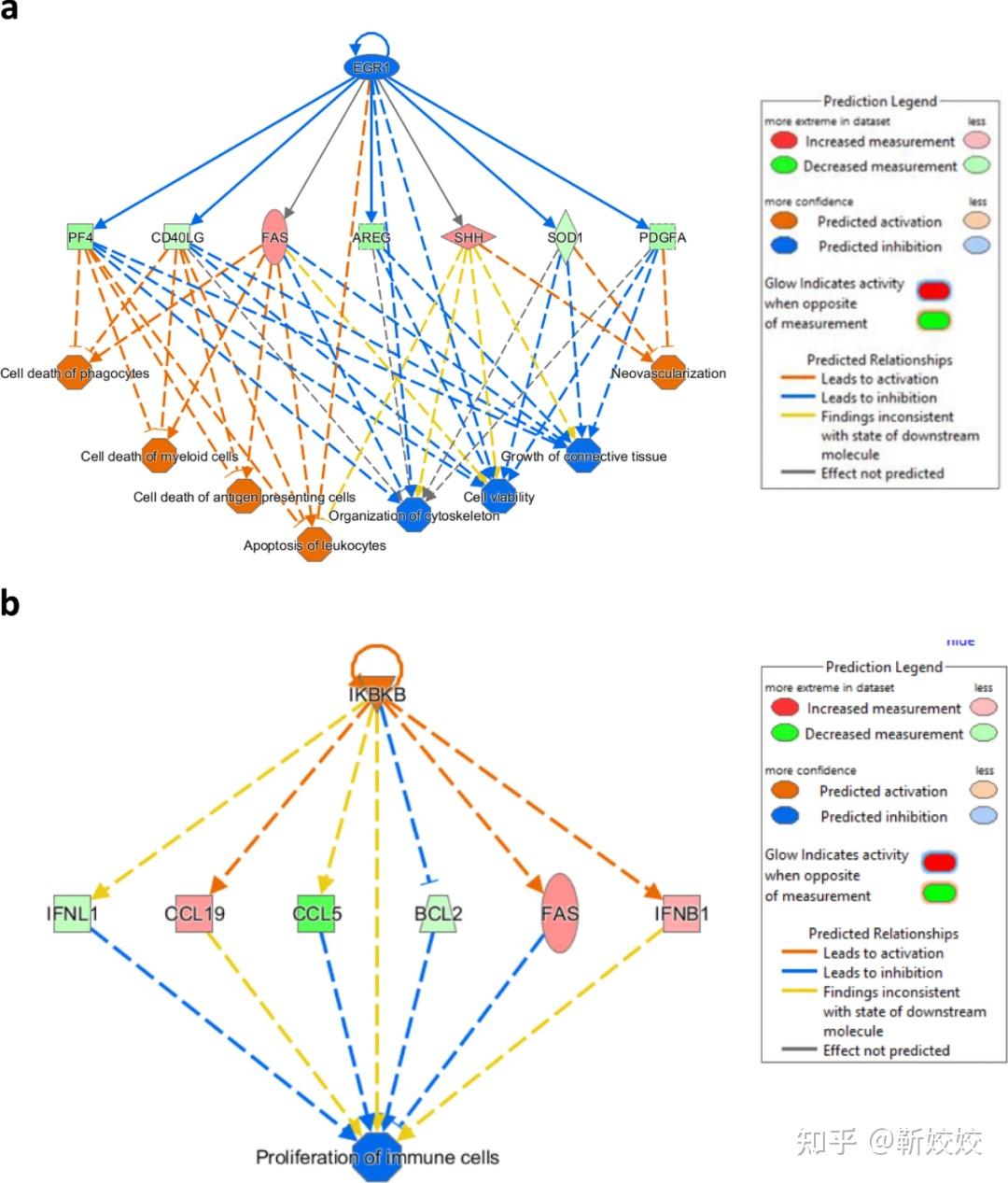
图4. 网络分析显示EGFR1相关的炎性细胞死亡以及IKB相关的免疫细胞增殖减少[10]
03
在心血管疾病风险预测与生物标志物中的应用
在一项涉及4个国际队列、约14145名来自全球不同国家、年龄和种族的个体的广泛研究中,研究人员开发并验证了一种基于血液中蛋白质水平的心肺健康(CRF)评分系统。通过LASSO统计学方法,从7230个候选蛋白质中筛选出272个与CRF显著相关的蛋白质。通过综合分析这些蛋白质,构建了一个名为“蛋白质CRF分数”的指标,该分数在预测多种临床结局(如死亡率、心血管疾病风险等)方面显示出强大的能力,并且有效改善了高遗传风险群体疾病风险的分类准确性[11]。另一项研究中,Perry等[12]通过测量多种环境暴露因素下的血浆蛋白质组,揭示了环境暴露相关的蛋白标志物与心血管事件及全因死亡率之间的显著关联,为理解环境因素对心血管健康的影响提供了新的视角。
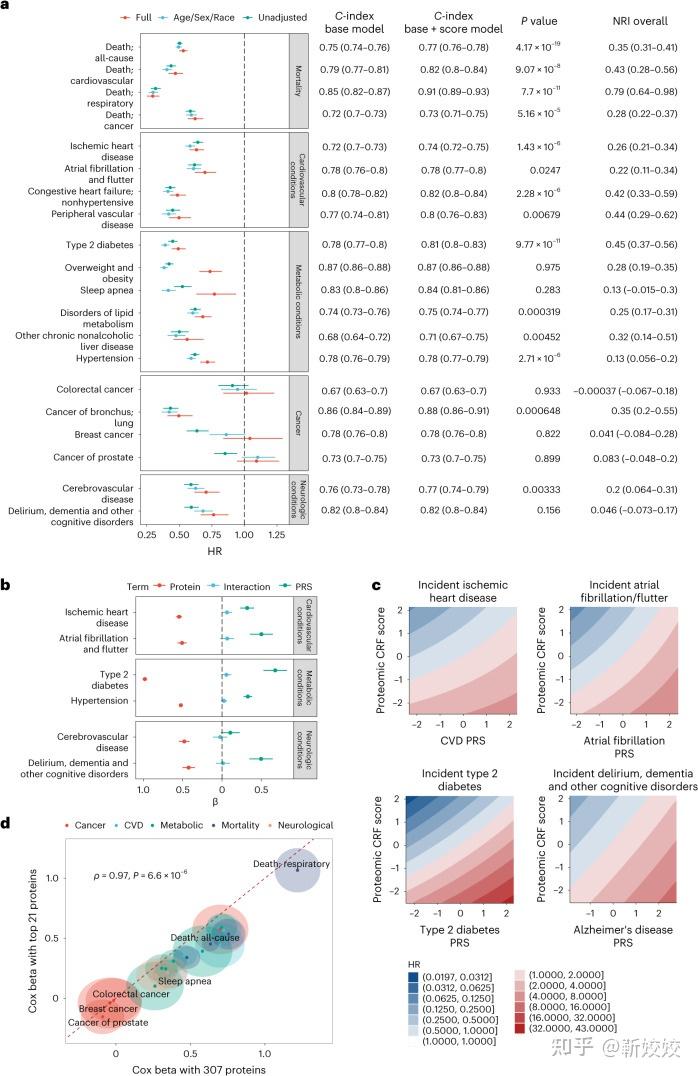
图5. 蛋白质组学CRF评分、多基因风险和多系统临床结果[11]
还有一项研究通过对比两组不同程度的人工诱导低血糖实验(一组轻度,一组重度,重度组随后给予葡萄糖以恢复血糖水平),探讨了低血糖对心血管风险蛋白标记物的影响及随后的恢复情况。研究结果显示,与对照组相比,仅在重度低血糖组中观察到ANGPT1和 DKK1的水平升高,且这些变化在低血糖得到纠正后消失。此外,在2型糖尿病患者中,低血糖期间BOC的表达出现下调,而即便在低血糖恢复后,其表达水平也并未出现明显回升。因此,该研究表明,尽管血糖的波动可能会对某些心血管风险标记物的水平产生短暂影响,但低血糖事件本身才是增加心血管事件风险的主要因素[13]。
另外,一项大规模血液蛋白质组学研究在群体动脉粥样硬化风险研究中发现了52种与主动脉瓣狭窄(AS)相关的蛋白质。这些蛋白质在晚年人群中高表达,与主动脉瓣功能下降及未来主动脉相关住院风险增加有关。其中,MMP12、C1QTNF1和GDF15与主动脉瓣钙化程度显著相关,并在心血管健康研究队列中得到验证。进一步分析显示,MMP12和血管内皮生长因子2在心脏病变组织中上调,提示参与主动脉硬化病理过程,为AS机制理解及新疗法开发提供了重要候选分子[14]。
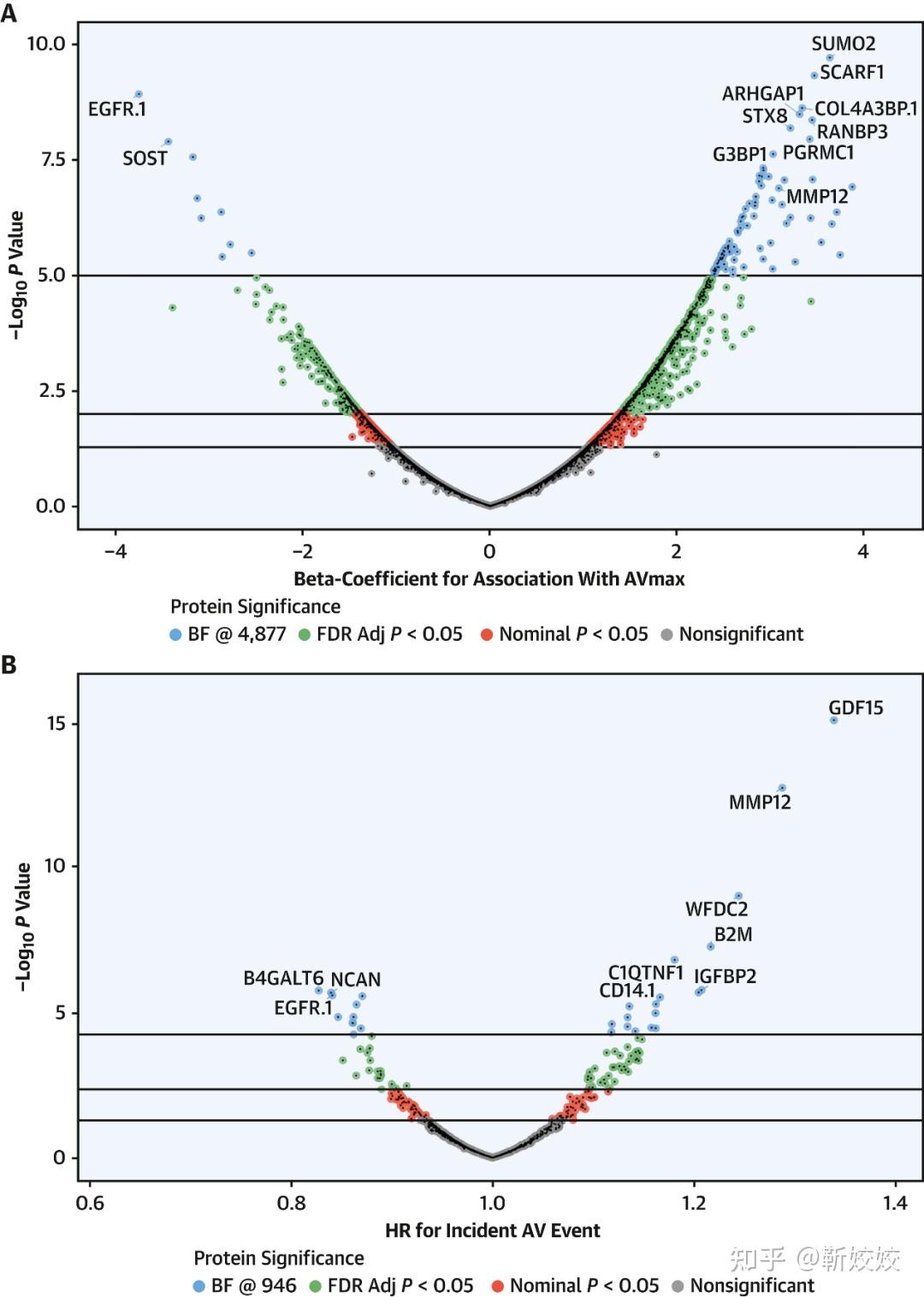
图6. 血浆蛋白质组学与房颤血流动力学和房颤相关住院治疗的关联[14]
此外,Akita等[15]通过一项多中心前瞻性队列研究,探讨了血清中10种特定脂联素(含抵抗素、瘦素、爱帕琳肽、脂联素等)水平与肥厚型心肌病(HCM)患者心脏性死亡的关系。研究纳入了哥伦比亚大学Irving医学中心和马萨诸塞州综合医院的389名HCM患者,分为训练集和测试集。结果显示,基于训练集的10种脂联素随机森林分类模型能有效预测测试集的心脏性死亡事件,高风险组心脏性死亡风险显著高于低风险组。该研究首次证明血清脂联素谱系可预测HCM患者心脏性死亡风险,有助于识别高风险患者并指导监测和干预措施的实施。
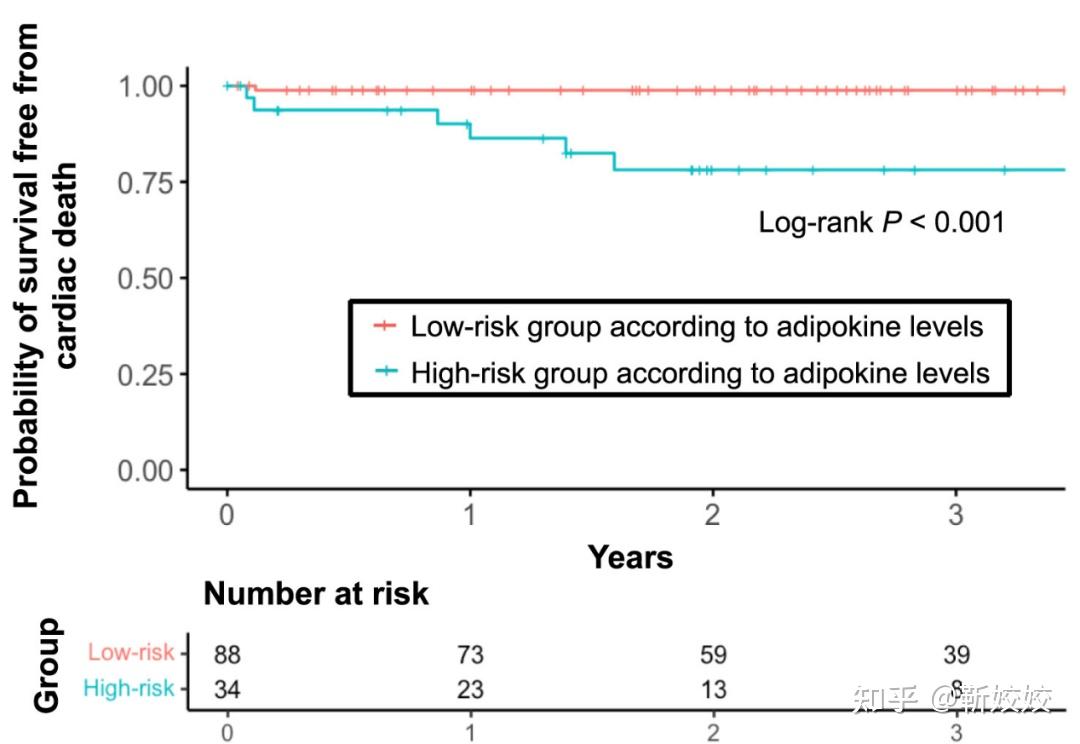
图7. 不同血浆脂联素水平组的生存曲线[15]
04
总结与展望
蛋白质组学检测在心血管疾病领域的应用研究取得了显著进展,为心血管疾病的发病机制研究、生物标志物发现、风险评估与预测以及药物治疗效果评估等提供了重要支持。未来,随着技术的不断进步和应用范围的扩大,蛋白质组学有望在心血管疾病的预防、诊断和治疗中发挥更加重要的作用。
参考文献
1.Lumish HS, et al. Comprehensive Proteomic Profiling of Human Myocardium Reveals Signaling Pathways Dysregulated in Hypertrophic Cardiomyopathy. J Am Coll Cardiol. 2024;84(20):1999-2011. doi: 10.1016/j.jacc.2024.07.043.
2.Lee C, et al. Signaling Pathways Associated With Prior Cardiovascular Events in Hypertrophic Cardiomyopathy. J Card Fail. 2024;30(3):462-72.doi: 10.1016/j.cardfail.2023.07.010.
3.Lumish HS, et al. Prediction of new-onset atrial fibrillation in patients with hypertrophic cardiomyopathy using plasma proteomics profiling. Europace. 2024;26(11).doi: 10.1093/europace/euae267.
4.Yuan S, et al. Proteomic insights into modifiable risk of venous thromboembolism and cardiovascular comorbidities. J Thromb Haemost. 2024;22(3):738-48.doi: 10.1016/j.jtha.2023.11.013.
5.Zhu Y, et al. Identification of pleiotropic and specific therapeutic targets for cardio-cerebral diseases: A large-scale proteome-wide mendelian randomization and colocalization study. PLoS One. 2024;19(5):e0300500. doi: 10.1371/journal.pone.0300500.
6.Shi K, et al. Identification of potential therapeutic targets for nonischemic cardiomyopathy in European ancestry: an integrated multiomics analysis. Cardiovasc Diabetol. 2024;23(1):338.doi: 10.1186/s12933-024-02431-8.
7.Chen L, et al. Systematic identification of therapeutic targets for coronary artery calcification: an integrated transcriptomic and proteomic Mendelian randomization. Front Cardiovasc Med. 2024;11:1419440.doi: 10.3389/fcvm.2024.1419440.
8.Alcalde-Herraiz M, et al. Effect of genetically predicted sclerostin on cardiovascular biomarkers, risk factors, and disease outcomes. Nat Commun. 2024;15(1):9832.doi: 10.1038/s41467-024-53623-5.
9.Abou Kamar S, et al. The plasma proteome is linked with left ventricular and left atrial function parameters in patients with chronic heart failure. Eur Heart J Cardiovasc Imaging. 2024;25(9):1206-15. doi: 10.1093/ehjci/jeae098.
10.Diakos NA, et al. Circulating Proteome Analysis Identifies Reduced Inflammation After Initiation of Hemodynamic Support with Either Veno-Arterial Extracorporeal Membrane Oxygenation or Impella in Patients with Cardiogenic Shock. J Cardiovasc Transl Res. 2024;17(4):935-45.doi: 10.1007/s12265-024-10501-1.
11.Perry AS, et al. Proteomic analysis of cardiorespiratory fitness for prediction of mortality and multisystem disease risks. Nat Med. 2024;30(6):1711-21.doi: 10.1038/s41591-024-03039-x.
12.Perry AS, et al. Proteomics, Human Environmental Exposure, and Cardiometabolic Risk. Circ Res. 2024;135(1):138-54.doi: 10.1161/CIRCRESAHA.124.324559.
13.Nandakumar M, et al. Effect of Hypoglycemia and Rebound Hyperglycemia on Proteomic Cardiovascular Risk Biomarkers. Biomedicines. 2024;12(6).doi: 10.3390/biomedicines12061137.
14.Shelbaya K, et al. Large-Scale Proteomics Identifies Novel Biomarkers and Circulating Risk Factors for Aortic Stenosis. J Am Coll Cardiol. 2024;83(5):577-91.doi: 10.1016/j.jacc.2023.11.021.
15.Akita K, et al. Prediction of cardiac death in patients with hypertrophic cardiomyopathy using plasma adipokine levels. Nutr Metab Cardiovasc Dis. 2024;34(6):1352-60.doi: 10.1016/j.numecd.2024.01.017.
SomaLogic公司推出的SomaScan Assay,作为一种基于aptamer(核酸适配体)的高通量蛋白质检测技术,专注于全面、精确地检测和测量人及其他模式动物血液、尿液等体液样本以及组织、细胞样本中的蛋白质组成。该技术旨在提高对健康和疾病生物学的理解,促进药物靶点的识别及生物标志物的开发,其检测范围覆盖超过11000种蛋白质,实现高通量蛋白质组学的检测和强大的数据分析,广泛应用于衰老、癌症、代谢性疾病、心血管疾病及神经退行性疾病的早期发现与监测中。
原文地址:https://zhuanlan.zhihu.com/p/21599339755 |
|
 /3
/3 