金桔
金币
威望
贡献
回帖0
精华
在线时间 小时
|
登陆有奖并可浏览互动!
您需要 登录 才可以下载或查看,没有账号?立即注册


×
1 背景知识介绍
显色原位杂交(Chromogenic in Situ Hybridization, CISH)或称原位显色杂交,与FISH技术原理一样,利用标记的互补DNA或RNA链在组织标本靶向特定DNA或RNA序列的过程,并实现靶基因可视化评估。一般情况下CISH作为免疫组化(immunohistochemistry, IHC)补充,在疾病检测或预防领域,当某种疾病还处于初级阶段时候,基因的表达较低,对应的蛋白丰度也较低,使用IHC评估的效果不理想,而使用CISH在基因层面进行评估更具有实践价值对指导预防治疗或疾病治疗十分重要。此外,对于一些诊断困难的疾病,可以使用IHC和CISH的结果对疾病进行比较精确的诊断。
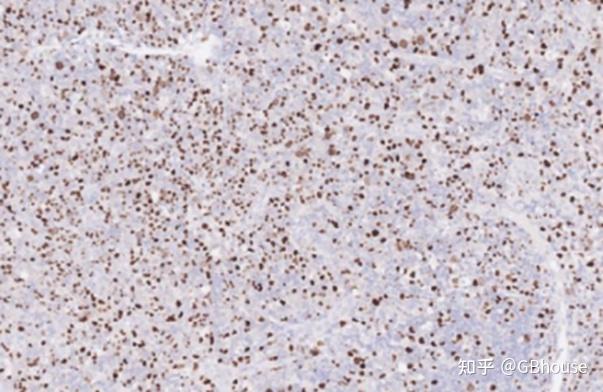
(图1 CISH评估组织EBV感染结果)
2 CISH与FISH比较
根据目前发表的文章来看,因FISH能够对同一样本中直观显示多个靶标,这一突出优点,使用的频率比较高。但CISH也有优于FISH的有点,尤其结合IHC在病理性诊断过程具有更实用的价值,例如检测样品保存时间不受限制,使用普通显微镜即可观察,组织形态评估,对IHC结果阴/阳辅证等。
表1不同原位杂交和ICH的异同[1]

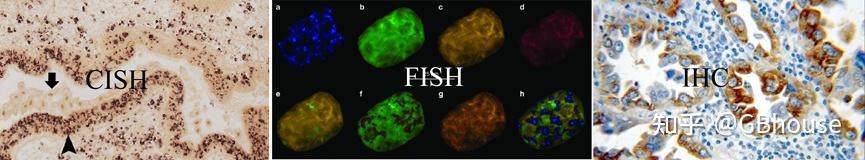
(图2 CISH,FISH和IHC实验结果呈现,可以明显的感受到FISH不论是放大倍数还是视觉冲击都是很棒的。对于分子机理探究使用FISH可能会更好,而对于疾病诊断只需要确定有无以及样本保存时间即可,使用IHC和CISH可能更实用)
3 CISH组织包埋
CISH的实验操作与IHC实验操作类似,各位朋友可以关注GBhouse推文《组织形态学免/疫组化免疫/荧光四部曲之----免疫组化(IHC)》和《组织形态学免疫组化免疫荧光四部曲(1)--组织包埋》 [3-5]。
3.1 组织固定于包埋
对于检测不同的定位的信号,使用的包埋试剂是存在差异的,尤其是对一些低表达的基因和低丰度当蛋白,对于CISH的固定使用3.7%甲醛[4]。下边就简单介绍一下,不同定固定剂的应用范围:
表2 不同固定剂的使用范围[1]

3.1 组织固定(以睾丸为例)
3.1 准备工作
3.1.1石蜡提前熬制(去除杂质和水分):
所用石蜡要求透明无杂质,新的石蜡要反复70℃熔凝(提前1-2天开始),将沉在底部的杂质除去,用吸水纸擦干净,包埋用过的石蜡要回收反复利用(但不可有组织污染)。烘箱加热(70℃,蜡的熔点约在58-60℃,此法熬的蜡是白色,但温度较低,需更早开始熬蜡,提前3-4天。要加热一周的时间,白天来的时候打开烘箱,晚上走的时候再关)。包埋前溶蜡,进口蜡65度烘箱,国产蜡68度烘箱。溶蜡时长约6小时(前一天采样)。
3.2 取样(1cm3左右)
小鼠睾丸,一般整个取样,需要使用注射器穿刺数次扎孔(10-20次左右)以便甲醛浸入,使不能破坏白膜,白膜上有空洞但不破坏内部组织(新的针头轻轻戳破白膜即可,刺孔个数根据睾丸大小来确定)。
3.3 固定(目的是为了固定蛋白,使蛋白变性)
直接将获得的整个睾丸组织使用3.7%甲醛进行固定,固定时间一般在96小时左右,即可完成甲醛对睾丸的作用,可用于后期实验。
3.4 脱水(脱去组织内水分)
3.4.1 固定组织漂洗
组织固定结束后,用PBS漂洗组织块3×30min(摇床)。目的:洗去渗入组织中的固定液,以免影响组织对组织内部结构的观察、分析、研究。
3.4.2 固定组织梯度脱水
依次用30%,50%,70%,80%,90%,100%(I),100%(II)(梯度脱水,一方面避免组织迅速脱水变性,细胞变形;另一方面使细胞表面与内部均一性脱水)进行漂洗,每次漂洗30min(一直洗到酒精的颜色不是很黄为止)。洗去绝大部分苦味酸浮色(80%以上酒精回收,倒入工业酒精桶,做酒精灯燃料)。在无水乙醇中时间不能太长,否则组织易碎/每次更换脱水剂,将组织块吸干
3.4.3 脱水组织保存
如实验安排原因无法立时完成后续步骤,此步可以经70%酒精后(不建议长期保存),将组织样品存放在75%酒精内,长期保存(长期保存要封口,每个月换一次75% 酒精)。或者对相同样品中的部分样品采取75% 酒精保存,后续另行使用。组织块在高浓度乙醇中,特别是无水乙醇内不能放置时间过长,因为高浓度乙醇吸水能力太强,易造成组织块过度硬化,使切片内组织易碎裂。
3.5 组织透明
使用80%,90%,100%(I),100%(II)二甲苯(使用无水乙醇进行配制)各30min,溶出组织内脂肪和多余的酒精。同时二甲苯处理会使组织变脆,时间过长不利于切片;时间过短脂肪残留,染料有可能结合不到蛋白上)(此处不同弄得的二甲苯使用无水乙醇进行配制)
透明过程中二甲苯将组织内脂肪和酒精溶出,组织变的透亮,故称为透明。注意事项:乙醇:二甲苯=1:1 浸泡组织2h(于15ml管内)进行预处理,用塑封袋封装后(因为二甲苯会挥发,防止二甲苯挥发进室内),置于摇床上。第一步透明,二甲苯(I),通透组织块5min;
第二步透明,更换新的二甲苯(II)(试验中所有的I II成分都一样,目的是多洗一次,让尽量纯净的液体进入细胞中),浸泡约10min(这一步的时间要自己把握,最凭经验的一步,观察通透至组织大部分呈透明样,注意不要使组织样颜色变过深变黑(透明过程既要尽量完全,又不能太过)。
3.6 浸蜡
浸蜡步骤去除组织中的二甲苯,支撑组织中细胞结构以便后期切片观察,以石蜡代替,浸蜡是否完全直接关系到切片完整。
3.6.1过渡
二甲苯:石蜡=1:1,浸泡组织块2h,(68℃烘箱,下同)。更换15ml管,要预热1h左右,再放入组织(可将石蜡、二甲苯倒入15ml管提前预热);利用二甲苯继续去除残留的脂肪 ,借助二甲苯与石蜡的互溶能力,将石蜡带到原脂肪填充位置,使得石蜡融进组织内 。
3.6.2 石蜡浸泡
石蜡(I,可能还含有二甲苯,重复使用的石蜡,也可以用全新的石蜡)浸泡组织块1h,去除组织块中二甲苯。
3.6.3 组织最终浸蜡
石蜡(II)(从石蜡I到石蜡II 一定要换容器,取出的样品要在纸上滚动一下,都是为了防止二甲苯污染)浸泡组织块2h, 充分去除组织中二甲苯。浸蜡期间,每过30min就要晃动一次15ml管,且烘箱中温度必须严格控制,浸蜡时间不能过长(我一般是浸蜡12-16h左右,即过夜),浸蜡时间或温度过长,会使组织收缩和脆变。
4 CISH组织块包埋
4.1 准备工作
浸蜡结束后,将组织块转移到已倒好石蜡的模具中,保证模具不会泄漏,组织块放入后,烘箱内放置30min以上,目的在于:使组织块内石蜡和包埋用石蜡充分互溶,以保证组织块完全包入石蜡同时做好样品标记(若不烘,组织块与蜡块结合不充分,切片时可能会分开)。

(图3 立样模具,建议使用这种具有塑性的模具,在蜡块凝固后更容易取出)
4.2 立样
针对小鼠睾丸,目的是最后可得到睾丸管腔的横切面,这也是整个实验的目的,如果得不到曲细精管的横切面,一切实验都是徒劳)为保证切片时切面为横向管腔,小鼠需要进行立样,使睾丸长轴垂直底面(也可以根据附睾定位睾丸的上下结构,进行上下立样),切记不能让睾丸长界面横躺在立样槽子中。操作时,动作迅速稳定,放置石蜡分层(立样用的镊子要提前放在烘箱中升温)。
4.3 冷却凝固
待睾丸稳定地立在底部后,将模具置于室温下,待冷凝完成,完成后取出蜡块,做好标记。(4℃冷却蜡块中间的凹陷会较深可能会暴露样品,一般常温凝固),自然冷凝完全(冬天一个晚上即12-16h左右,夏天可以延长至24h)。凝固以后使用压脉带(也就是平时医院包扎伤口时候用到的布制胶带)。

(图4 收集凝固的石蜡块,标记清楚物种,组别,组织名称。)
5 CISH切片
5.1切片前修蜡
待蜡块凝固完全后,将蜡块从模具中取出,做好标记。 切片前需对蜡块进行修整,去除组织周围多余石蜡,注意保留组织完整,我喜欢切成宝塔状。

(图5 修整蜡块,修成“宝塔状”,这样子有利于切片到最后的时候,不至于将整个组织块切下来,这是来自曾经失败的经验)
5.2切片准备
切片前准备载玻片:清洗干净,先在酸缸中清洗,随后用0.01%多聚赖氨酸(使组织与玻片更好地贴合)孵育15分钟,干燥保存(目前可以购买相关成品的载玻片,可不需要这么繁琐的操作,使用前提前咨询厂家)。切片刀、毛笔、小镊子、玻片架、标记用铅笔、水1L、卫生纸若干。展片水浴锅提前调整到42℃,展片时间必须严格控制(1-2min),否则会导致睾丸生殖细胞/支持细胞从睾丸基底膜脱落。捞片时,须在片子上标明制作人,样品制作时间,组织名称,切片厚度(一般是5-7μm,对于大组织或者比较容易皱缩的组织可适当增加厚度,不超过10μm)。
5.3切片
(1)用刀要小心,切片前一定要确认所有的旋钮都已固定死。
切片在10μm以下,免疫组化等的片子7μm,也可5μm。
(2)切片越薄切出的蜡片越容易形成褶皱,所以利用水的表面张力在水中展片。
(3)切片后毛笔向下、向外边转动边拉。
(4)若切出的一串拉片中有质量不好的蜡片,用手术刀,靠刀片轻轻的转动切断蜡片,注意不能能损伤台座。
(5)清除杂质时,毛笔向上扫,千万不能向下扫。否则会在刀片上形成划痕,这样切出的组织上也有划痕,染色会有问题。
(6)切出的蜡片呈扇形,多半是因为刀片上有豁口,移动一下刀片。或者就是蜡没有融好,密度不均一。
(7)切出的蜡片往回卷,因为有静电。可以事先用75% 酒精擦刀台面,固定蜡块的部位以及蜡块。
(8)用镊子夹蜡片的时候不能用力夹,否则蜡片会粘在镊子上。要虚着夹。
(9)切完后再用毛笔把蜡片展开。
(10)注意要匀速地转动摇柄,不能过快。
(11)连续切片基本是同一状态的细胞,同一视野。可以用不同的抗体染色,最后的图组合在一起。若要取多个不同视野观察,可以空切10刀。
(12)蜡块在切之前一定要固定好卡紧,否则蜡块会转动不利于切片。
(13)使用完机器后要收回固定蜡的装置,上方红绿色长方块消失(用小柄转,一个黑点是一倍,即小柄转一圈相当于大柄转十圈;两个黑点是两倍,即小柄转一圈相当于大柄转二十圈)。
(14)切完后先取刀片,再取蜡块,然后用软的卫生纸擦刀台面(刀片用65℃水煮,烘箱烘干除蜡),最后把整个台座都卸下来,将蜡的碎屑清除干净。
(15)水浴锅中倒入的是蒸馏水,或者自来水,42℃。
(16)片子内各组织尽量离开一段距离,方便做免疫组化时阻断笔分开。
(17)片子标注:首先写组织名称,再写样品时间、样品归属人,切片厚度。
(18)切片尽量保证一张载玻片上4个左右组织方向一致,在水平线上。
6 CISH操作[4]
(1)组织切片干燥,将4-5μm 厚的组织安装在组织载玻片上,在37℃ 干燥,并在60℃干燥2-4小时;
(2)组织脱蜡,载玻片在室温(22-27℃)下在二甲苯中脱石蜡15分钟3次,室温下在100% 乙醇中洗涤2分钟3次;
(3)SPOT-Light孵育,将它们在37 ℃ 下用100μl SPOT-Light 组织预处理酶覆盖10分钟,后在室温下在 PBS 中洗涤2分钟3次;
(4)组织切片脱水,使用梯度酒精(70% ,85% ,95% 和100%)脱水2分钟每次,然后风干;
(5)探针孵育,将变性探针(15μl)加入到每个样品的中心,并用24 mm × 32 mm 盖玻片覆盖,其边缘用薄层橡胶粘合剂密封以防止在孵育期间探针溶液的蒸发,将载玻片在94 ℃下变性3分钟,并在37 °C 下置于暗湿箱中16-24小时;
(6)组织切片洗涤,取出胶粘剂和盖玻片后,将载玻片在75℃ 的水浴中浸泡在0.5 × SCC 缓冲液中5分钟,然后将它们在 PBS-Tween 20缓冲液中在室温下洗涤2分钟3次;
(7)组织切片封闭,载玻片浸泡在过氧化物酶淬灭液中,用 PBS 洗涤2分钟3次,然后用试剂 A(100 μl of CAS Block) 进行内源性生物素封闭;
(8)组织切片标记,使用 Zymed 的 SPOT-Light 检测试剂盒,将100μl 异硫氰酸荧光素标记的绵羊抗地高辛,辣根过氧化物酶标记的山羊抗异硫氰酸荧光素和二氨基联苯胺发色团依次加入到载玻片中,在加入试剂之间用 PBS-Tween 漂洗3次2分钟;
(9)载玻片用150μlGill-2苏木精复染并温育3分钟。然后用一系列不同级别的酒精使它们脱水,在二甲苯中孵育1min,使用中性树脂封片;
(10)观察与数据采集,使用显微镜进行观察和图片数据采集。
7 结束。
爱自己!!!做科研!!! 每文格言“诺贝尔文学奖得主,奥尔罕·帕穆克:其实我希望你对我说谎,因为人只为了非常害怕失去的一样东西才说谎。”如果有用,关注楼主GBhouse,点赞+讨论,攻击型人格请请请不要关注和阅读!!!
参考
[1]https://www.thermofisher.cn/cn/zh/home/life-science/cell-analysis/cellular-imaging/in-situ-hybridization-ish.html
[2]https://ptglab.biomart.cn/news/3155639.htm#:~:text=%E5%8F%AF%E6%BA%B6%E6%80%A7%E6%BA%B6%E5%89%82%E6%AF%94%E5%A6%82%E4%B8%99%E9%85%AE%E3%80%81%E4%B9%99%E9%86%87%E7%AD%89%E8%83%BD%E5%8E%BB%E9%99%A4%E8%84%82%E7%B1%BB%E7%89%A9%E8%B4%A8%E5%B9%B6%E4%BD%BF%E7%BB%86%E8%83%9E%E8%84%B1%E6%B0%B4%EF%BC%8C%E6%8A%8A%E8%9B%8B%E7%99%BD%E8%B4%A8%E6%B2%89%E6%B7%80%E5%9C%A8%E7%BB%86%E8%83%9E%E7%BB%93%E6%9E%84%E4%B8%8A%E3%80%82,%E4%BA%A4%E8%81%94%E5%89%82%E6%AF%94%E5%A6%82%E5%A4%9A%E8%81%9A%E7%94%B2%E9%86%9B%E5%8F%AF%E4%BB%A5%E9%80%9A%E8%BF%87%E8%87%AA%E7%94%B1%E6%B0%A8%E5%9F%BA%E5%9F%BA%E5%9B%A2%E6%8A%8A%E7%94%9F%E7%89%A9%E5%88%86%E5%AD%90%E6%A1%A5%E8%BF%9E%E8%B5%B7%E6%9D%A5%EF%BC%8C%E5%BD%A2%E6%88%90%E4%B8%80%E4%B8%AA%E7%9B%B8%E4%BA%92%E8%BF%9E%E6%8E%A5%E7%9A%84%E6%8A%97%E5%8E%9F%E7%BD%91%E3%80%82%20%E7%BB%84%E7%BB%87%E6%88%96%E7%BB%86%E8%83%9E%E7%BB%8F%E8%BF%87%E5%9B%BA%E5%AE%9A%E5%90%8E%E5%8F%AF%E4%BD%BF%E8%83%9E%E5%86%85%E8%9B%8B%E7%99%BD%E5%87%9D%E5%9B%BA%EF%BC%8C%E5%87%8F%E5%B0%91%E6%88%96%E7%BB%88%E6%AD%A2%E5%A4%96%E6%BA%90%E6%80%A7%E9%85%B6%E5%92%8C%E5%86%85%E6%BA%90%E6%80%A7%E9%85%B6%E7%9A%84%E5%8F%8D%E5%BA%94%EF%BC%9B%E4%BF%9D%E6%8C%81%E7%BB%84%E7%BB%87%E6%88%96%E7%BB%86%E8%83%9E%E7%9A%84%E6%8A%97%E5%8E%9F%E6%80%A7%EF%BC%8C%E9%81%BF%E5%85%8D%E6%8A%97%E5%8E%9F%E5%8F%91%E7%94%9F%E5%BC%A5%E6%95%A3%EF%BC%9B%E4%BF%9D%E6%8C%81%E7%BB%84%E7%BB%87%E5%92%8C%E7%BB%86%E8%83%9E%E7%9A%84%E5%9B%BA%E6%9C%89%E5%BD%A2%E6%80%81%E5%92%8C%E7%BB%93%E6%9E%84%E3%80%82
[3] https://www.biosb.com/biosb-products/zytodot/
[4] Madrid MA, Lo RW. Chromogenic in situ hybridization (CISH): a novel alternative in screening archival breast cancer tissue samples for HER-2/neu status. Breast Cancer Res. 2004;6(5):R593-600. doi: 10.1186/bcr915. Epub 2004 Jul 29. PMID: 15318940; PMCID: PMC549176.
[5] Tanner M, Gancberg D, Di Leo A, Larsimont D, Rouas G, Piccart MJ, Isola J. Chromogenic in situ hybridization: a practical alternative for fluorescence in situ hybridization to detect HER-2/neu oncogene amplification in archival breast cancer samples. Am J Pathol. 2000 Nov;157(5):1467-72. doi: 10.1016/S0002-9440(10)64785-2. PMID: 11073807; PMCID: PMC1885742.
[6] Hanna WM, Kwok K. Chromogenic in-situ hybridization: a viable alternative to fluorescence in-situ hybridization in the HER2 testing algorithm. Mod Pathol. 2006 Apr;19(4):481-7. doi: 10.1038/modpathol.3800555. PMID: 16444193.
原文地址:https://zhuanlan.zhihu.com/p/711426219 |
|
 /3
/3 