金桔
金币
威望
贡献
回帖0
精华
在线时间 小时
|
目前癌症的液体活检发展如何?我们距离“验血测癌”还有多远?
在癌症早期,患者往往缺乏明显的特征性症状,而发现时癌症常常已经转移。这也是当前多种癌症致死率居高不下的一个重要原因。因此,实现早期筛查是提升癌症患者生存率的关键。
在液体活检中,最常见的检测目标是循环无细胞DNA(cfDNA)。cfDNA是游离在血浆中的DNA片段,这些长度只有大约150个碱基对的片段通常来自正常组织,但对于癌症患者,他们体内的癌细胞也会贡献其中的一小部分cfDNA。而这些包含了与癌症相关的突变的DNA片段,就成了液体活检的主要检测对象。
不过,基于液体活检的检测工具开发并不顺利。一方面,早期癌症患者释放至血浆中的DNA片段含量较低,极端情况下cfDNA中只有不到0.1%来自癌细胞,要检测出癌细胞的DNA片段绝非易事。另一个问题则是存在假阳性:除了癌症,血细胞的良性增殖也可能产生突变,这种“意义不明的克隆性造血”也可能被误认为是癌症信号。此外,由于不同部位的癌症可能产生相似的信号,因此难以辨别癌细胞的来源。
图片来源:123RF
面对这样的局面,最近几年,一些研究开始尝试新策略。其中一种,便是引入蛋白标志物的检测。
2018年,约翰·霍普金斯大学的研究团队发表了一篇革命性的《科学》论文。这项研究将cfDNA测序和与癌症相关的血清蛋白标志物结合,开发出了一个用于筛查癌症并明确癌症组织来源的算法。通过对16个基因和8个蛋白质的检测,这个名为CancerSEEK的算法能检测出8种不同类型的癌症。在对上千名癌症患者的测试中,CancerSEEK的平均检出率为70%,其中对卵巢癌和肝癌的检出率高达98%。而对健康志愿者血液样本的检测显示,检测的特异性超过了99%,即有效地避免了假阳性。
两年之后,CancerSEEK更进一步。在另一项发表于《科学》的前瞻性研究中,CancerSEEK的检测对象换成近万名未出现症状的健康女性,以模拟现实世界的情况。结果,CancerSEEK共检测出26位传统方法没有发现的癌症患者。这些癌症病例包含10种类型,其中7种(例如卵巢癌、肾癌)缺乏通过批准的传统筛查手段。
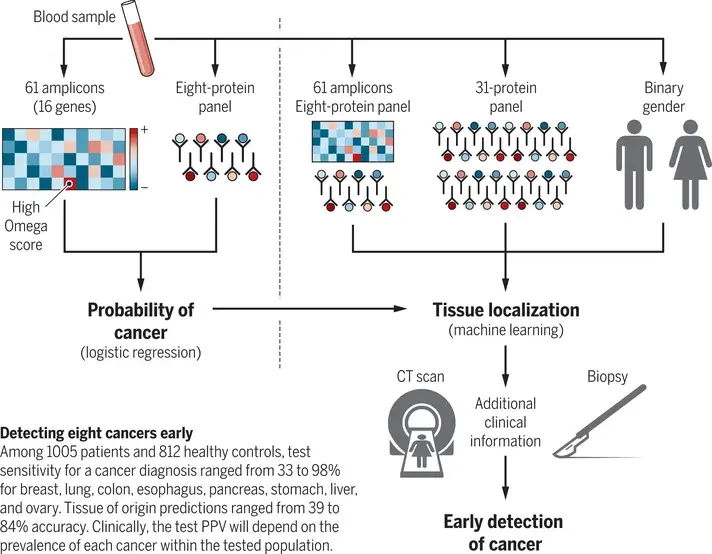
▲CancerSEEK算法工作原理(图片来源:参考资料[4])
另一方面,传统筛查手段另外筛查出了22位癌症患者。因此,将CancerSEEK与传统的筛查手段结合使用,可以将筛查出的癌症病例翻倍。这项研究同样展现出了较低的假阳性率。单独使用CancerSEEK共检测出101例假阳性,假阳性率约为1%;结合PET-CT后,假阳性率下降至不足0.4%。
另一种液体活检策略是检测DNA甲基化特征。对于癌症患者,DNA甲基化变化数量众多并且分布的位点丰富,这样的特征能提升液体活检的灵敏性。而不同组织发育过程中甲基化特征不同,因此通过检测甲基化特征来判断DNA的组织来源,应该也具有足够的特异性。
2020年,一项发表于《肿瘤学年鉴》的研究就通过1.5万人的试验发现,该方法对于早、中期癌症的整体检测率为44%,检测的特异性达到99.3%,并且能判断出93%的已知癌症的位点。
那么,这些突破距离真正为我们所用还有多远?
事实上,无论是Thrive Early Detection公司开发的CancerSEEK,还是GRAIL公司对于DNA甲基化的检测结果,都已经获得了FDA授予的突破性医疗器械认定,并且更多大型试验也在进行中。此外,我们也能看到其他企业与研究机构,正通过各自的方式尝试实现癌症的液体活检。或许距离这些检测工具最终获批上市,还有一些临床试验与几年时间,但只有脚踏实地、用数据说话,才能打造出真正可靠的筛查工具。
参考资料:
[1] Joshua D. Cohen et al. Detection and localization of surgically resectable cancers with a multi-analyte blood test. Science (2018). https://www.science.org/doi/full/10.1126/science.aar3247
[2] Anne Marie Lennon et al. Feasibility of blood testing combined with PET-CT to screen for cancer and guide intervention. Science (2020). https://www.science.org/doi/full/10.1126/science.aar3247
[3] M.C. Liu et al. Sensitive and specific multi-cancer detection and localization using methylation signatures in cell-free DNA. Annuals of Oncology (2020). https://www.annalsofoncology.org/article/S0923-7534(20)36058-0/fulltext
[4] Mark Kalinich et al. Cancer detection: Seeking signals in blood.Science (2018). https://www.science.org/doi/10.1126/science.aas9102▎药明康德内容团队编辑
本文来自药明康德内容团队,欢迎转发到朋友圈,谢绝转载到其他平台。
免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
⤵️喜欢我们的内容,欢迎关注@药明康德!或者点赞、评论、分享给其他读者吧! |
|
 /3
/3 