在临床诊断和生物医学研究中,低丰度蛋白质的精准检测一直是“皇冠上的明珠”。哈佛大学David R. Walt团队曾在《ACS Nano》发表两篇重要文献,推出了MOSAIC技术,通过两次关键突破,实现了对传统Simoa技术的超越,描绘了蛋白质检测技术向高灵敏度、高通量迈进的宏伟蓝图。
打破Simoa局限:低丰度蛋白检测的挑战
尽管Simoa技术通过将单个免疫复合物隔离在微孔中,实现了亚飞摩尔级别的灵敏度,但它仍面临采样效率低、设备门槛高、多重检测受限等痛点。Simoa分析时仅能覆盖约5%的磁珠,导至在极低浓度下受泊松噪声影响大,灵敏度提升遭遇瓶颈,同时依赖昂贵的定制化设备。 MOSAIC 1.0:超高灵敏度与高通量的完美结合2022年,Walt团队推出了初代MOSAIC技术,核心原理为“原位放大+流式读取”。利用过量抗体包被的磁珠捕获目标蛋白,通过链霉亲和素-DNA偶联物引发滚环扩增(RCA),在磁珠表面直接生成长长的DNA串联体。随后使用常规流式细胞仪即可快速区分并进行精准计数。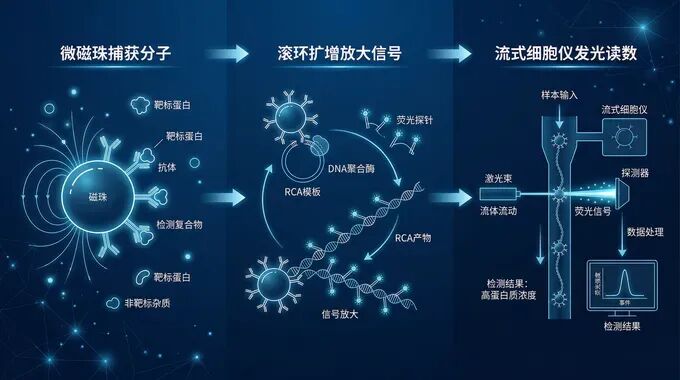 相比于Simoa,初代MOSAIC将采样效率从5%飙升至50-60%,检测限低至attomolar级别,比Simoa提高了3-12倍。此外,它摒弃了复杂的微孔加载过程,仅需实验室常见的流式细胞仪,打破了微孔数量的物理限制,理论上可实现更高维度的多重检测。 条码MOSAIC:攻克多重检测的交叉反应难题初代MOSAIC虽然打开了高多重检测的大门,但随着同时检测的分析物数量增加,抗体交叉反应成为亟待解决的难题。不同靶标的检测抗体极易发生“串门”,结合到非目标蛋白上,导至严重的假阳性,影响了超高灵敏度检测的准确性。 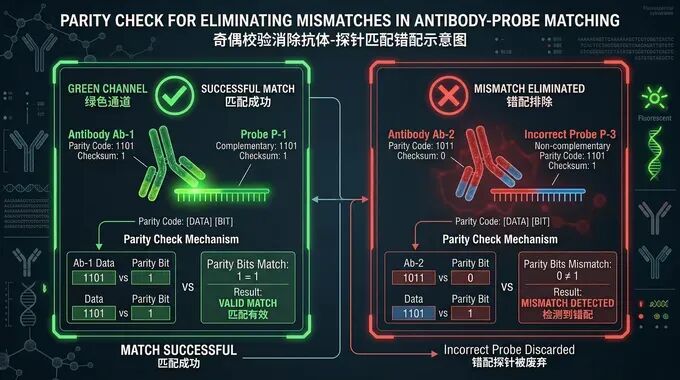
为解决此问题,2024年团队推出了“条码MOSAIC”。通过DNA条码标记和奇偶校验策略,只有当捕获珠类型与探针荧光信号绝对完美匹配时,珠子才会被判定为阳性。在临床验证环节,条码MOSAIC仅用不到25μL的稀释血浆,就精确完成了包含CA-125等5种癌症标志物的定量分析,只需不到17μL血浆,即可同时检测浓度跨越picomolar到attomolar的8种癌症相关蛋白。 
从Simoa到MOSAIC的技术演进,是一场不断突破检测极限与应用瓶颈的革命。MOSAIC技术的出现带来了深远的科学与临床意义,不仅实现了技术的真正普及化,还成为液体活检与早期诊断的利器。
参考文献:
[1] Wu C, Dougan TJ, Walt DR. High-Throughput, High-Multiplex Digital Protein Detection with Attomolar Sensitivity. ACS Nano. 2022Jan25;16(1):10251035.doi:10.1021/acsnano.1c08675.Epub2022Jan14.PMID: 35029381; PMCID: PMC9499451. [2] Zhang SJ, Wu C, Walt DR. A Multiplexed Digital Platform Enables Detection of Attomolar Protein Levels with Minimal Cross-Reactivity. ACS Nano. 2024 Oct 29;18(43):29891-29901.doi: 10.1021/acsnano.4c10340.Epub 2024 Oct 18.PMID: 39422558.
|  /3
/3 